 资源简介
资源简介
人教版九年级化学第五单元
课题1 质量守恒定律
课题1 质量守恒定律
一、教学目标
知识与技能
1、认识质量守恒定律,了解常见化学反应中的质量关系。
2、能从微观的角度解释质量守恒的原因。
过程与方法
1、通过小组讨论、选择装置,设计实验方案、进行实验、分析实验数据等一系列过程,初步体验定量研究化学反应的过程。
2、通过生生、师生间的讨论交流,理解质量守恒定律的实质,提高分析及推理能力。
情感态度与价值观
通过实验探究,初步养成严谨求实的科学态度。
二、教学重难点
教学重点:通过实验探究认识质量守恒定律。
教学难点:测定装置的选择和实验数据的处理。
三、教学过程
教学环节 教 师 活 动 学 生 活 动 设计思想
创设情境 展示冰块请用分子、原子的观点解释:冰变为水,变化前后总质量没有改变的原因。水通电变成了氢气和氧气,各物质的质量发生了什么变化?反应物的总质量和生成物的总质量是什么关系呢? 冰变为水的过程中水分子不变,只是分子间隔发生变化水的质量减少,氢气、氧气质量增加 开篇让学生初步建立宏观与微观的联系,为从微观粒子的角度解释质量守恒做铺垫。明确研究主题。
环节一实验探究环节一实验探究 水电解装置比较复杂,我们选一个较熟悉的反应进行研究。任务1请你设计实验装置探究测定磷与氧气的总质量和五氧化二磷的质量是否相等? 演示红磷燃烧实验过渡:刚才称得的物质都参加化学反应了吗?本质上到底是哪些物质的质量总和相等呢?引导学生对称得的数据进行分析得到初步的结论 思考,在教师的引导下考虑反应物中有气体,需使用密闭装置。描述实验现象反应前后总质量相等参加反应的磷的质量和参加反应的氧气的质量之和等于生成的五氧化二磷的质量。参加化学反应 m反应物总=m生成物总 从熟悉的反应出发,便于学生根据反应物和生成物的特点设计实验装置,考虑到反应物中有气体,设计密闭的实验装置。通过引导学生分析数据,让学生真正体会“参加”的含义,初步得到参加化学反应的各物质的质量总和等于生成的各物质的质量总和,提高学生的分析归纳能力,体验定量研究化学反应的过程。
其它的化学反应前后物质的总质量也是不变的吗?任务2请你选择装置探究该反应前后物质的总质量是否相等。 药品:碳酸钠和稀盐酸,仪器:电子秤、烧杯、矿泉水瓶、小试管、药匙。提示:1.矿泉水瓶、烧杯均可作反应装置,注意:碳酸钠(Na2CO3)取半药匙,盐酸(HCl)取半试管。2.将仪器和药品一起放在电子秤上称量。仿照对红磷燃烧反应前后等量关系的数据分析,描述碳酸钠与盐酸反应前后的等量关系。 学生讨论, 选择装置设计实验方案进行实验学生汇报参加反应的碳酸钠和参加反应的氯化氢的质量之和等于生成的氯化钠、二氧化碳和水的质量之和。 为研究化学反应前后物质的总质量是否相等再提供一个佐证。让学生的思维动起来,通过小组讨论和教师引导,考虑到生成物中有气体,要把生成物的质量全部称量,学会对装置的选择方法----有气体参加反应或有气体生成的反应要使用密闭装置,在师生交流和讨论中突破难点。
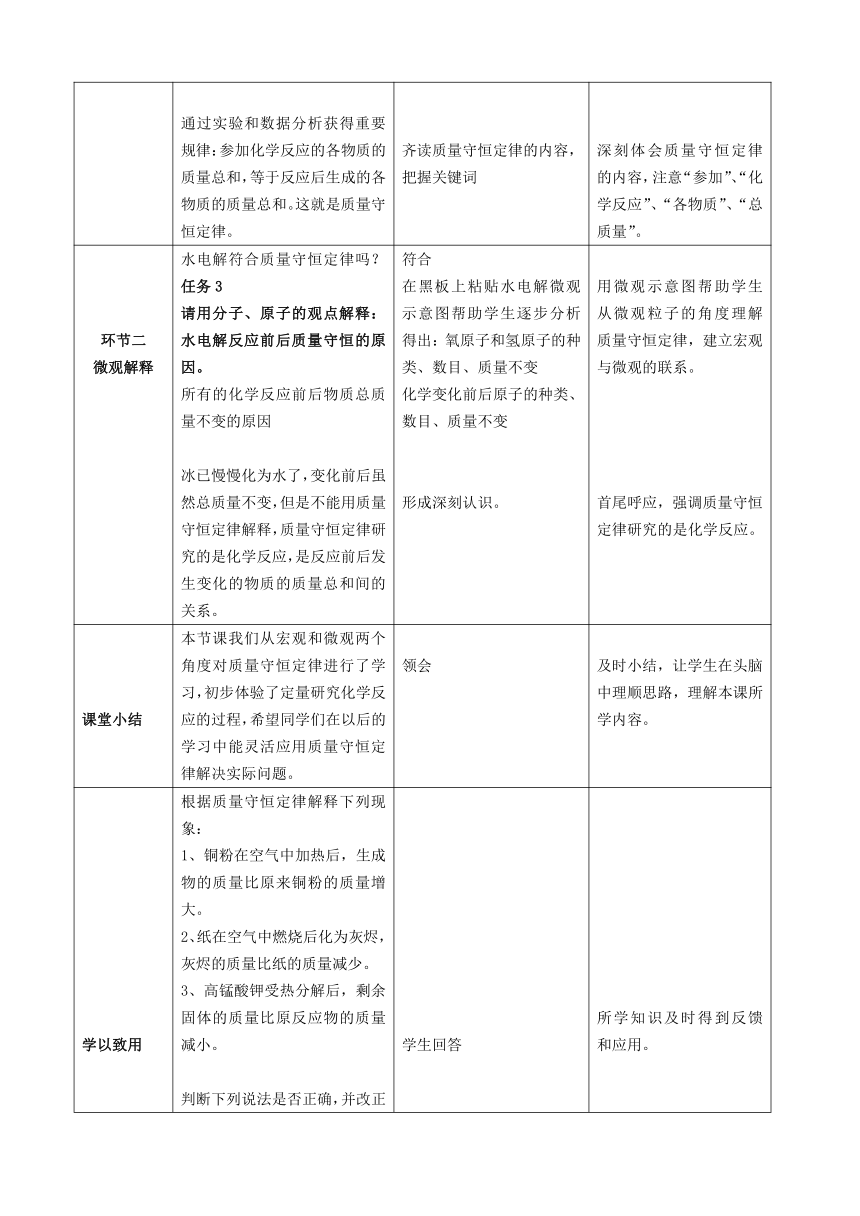
通过实验和数据分析获得重要规律:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这就是质量守恒定律。 齐读质量守恒定律的内容,把握关键词 深刻体会质量守恒定律的内容,注意“参加”、“化学反应”、“各物质”、“总质量”。
环节二微观解释 水电解符合质量守恒定律吗?任务3请用分子、原子的观点解释:水电解反应前后质量守恒的原因。 所有的化学反应前后物质总质量不变的原因冰已慢慢化为水了,变化前后虽然总质量不变,但是不能用质量守恒定律解释,质量守恒定律研究的是化学反应,是反应前后发生变化的物质的质量总和间的关系。 符合在黑板上粘贴水电解微观示意图帮助学生逐步分析得出:氧原子和氢原子的种类、数目、质量不变化学变化前后原子的种类、数目、质量不变形成深刻认识。 用微观示意图帮助学生从微观粒子的角度理解质量守恒定律,建立宏观与微观的联系。首尾呼应,强调质量守恒定律研究的是化学反应。
课堂小结 本节课我们从宏观和微观两个角度对质量守恒定律进行了学习,初步体验了定量研究化学反应的过程,希望同学们在以后的学习中能灵活应用质量守恒定律解决实际问题。 领会 及时小结,让学生在头脑中理顺思路,理解本课所学内容。
学以致用 根据质量守恒定律解释下列现象:1、铜粉在空气中加热后,生成物的质量比原来铜粉的质量增大。2、纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量减少。3、高锰酸钾受热分解后,剩余固体的质量比原反应物的质量减小。判断下列说法是否正确,并改正错误的说法 4、物质在空气中加热发生反应后,生成物的总质量必定等于反应物的总质量。5、蜡烛燃烧后的质量减小,说明质量守恒定律不是普遍规律。6、细铁丝在氧气中燃烧后,生成物的质量比细铁丝的质量大,因此这个反应不遵守质量守恒定律。 学生回答 所学知识及时得到反馈和应用。
布置作业 设计实验证明蜡烛燃烧符合质量守恒定律 课下思考并完成 对课堂所学知识的巩固和延伸。
四、板书设计
课题1 质量守恒定律
一、内容 参加化学反应 m反应物总=m生成物总 宏观
二、实质 原子的种类、数目、质量不变 微观
课题1 质量守恒定律
实验报告单
组长: 实验分工:称量: 记录
化学反应:碳酸钠 + 盐酸 → 氯化钠 + 二氧化碳 + 水
(Na2CO3) (HCl) (NaCl) (CO2) (H2O)
任务
请你选择装置探究碳酸钠与盐酸反应前后物质的总质量是否相等。
提供药品及仪器
药品:碳酸钠(Na2CO3)和盐酸(HCl)
仪器:电子秤、矿泉水瓶(盛Na2CO3)、烧杯(盛Na2CO3)、小试管(盛盐酸)、药匙。
提示:
1.矿泉水瓶、烧杯均可作反应装置,注意碳酸钠(Na2CO3)取半药匙,盐酸(HCl)取半试管。
2.将仪器和药品一起放在电子秤上称量。
请选择装置,设计实验方案,进行实验。
简要实验步骤 实验结果记录 实验结果分析
实验现象: m反应物总 m生成物总
反应前称量总质量(m1)为 g 反应后称量总质量(m2)为 g
展开更多......
收起↑
 资源预览
资源预览


 资源预览
资源预览


