 资源简介
资源简介
“质量守恒定律(第三课时)——化学方程式”教学设计
课题 质量守恒定律(第三课时)——化学方程式
课型 原理课
文献综述
《广州市义务教育阶段学科学业质量评价标准(化学)》中关于“质量守恒定律(第二课时)——化学方程式”的学业水平达标要求有以下表述:
知识与技能目标:
1、知道化学方程式是描述化学变化的语言。化学变化过程中,反应物和生成物的组成(即质的关系)、各物质间量的关系、反应条件、部分反应现象等都可以通过化学反应方程式用简洁的语言加以描述。
2、能从“质”与“量”的角度说出化学方程式的含义,根据化学方程式列举化学反应的有关信息。
过程与方法目标:
通过学习化学方程式,体会化学语言在化学研究中的重要作用,增强规范使用化学语言的意识。
情感态度与价值观目标
通过从“质”和“量”的角度对化学变化的认识,初步感受化学反应中,“量”的变化是由于“质”的变化引起的,而“质”的变化又始终是在“量”的守恒中进行的。体会“变”与“不变”的矛盾和统一,增进对辩证唯物主义观点的认识,进一步丰富物质的变化观。[1]
本人的教学目标与上述标准基本一致。本人的目标在文字、图形和化学方程式表述化学反应建立化学反应微观、宏观与化学方程式三重表征的联系。关于化学反应现象与化学方程式的关系本人在教学设计有体现,但没有设置在教学目标中。
闫亚瑞等人对国内外有关化学方程式教学研究进行综述,发现学生的理解按照宏观、微观、符号的顺序依次降低,接近一半学生对化学方程式中化学式的下标和系数的理解有不同程度的混淆,对于微观图和化学方程式的转换只考虑到方程式两边的原子个数应当相等,只注意了微粒图和方程式的表面特征,而没有理解化学方程式的实质过程。教师教学大多习惯于花费大量时间去训练学生的技能技巧,而没有将化学方程式所承载的丰富信息揭示出来。课堂教学应引导他们挖掘知识背后的内涵,深入理解化学方程式的内在含义。[6]刘萍认为化学方程式的学习要以兴趣教学法增强学习效果和巧妙降低教学难点来突破。[7]王少卿等人认为要结合化学实验的原理、装置、流程理解化学方程式,然后将符号表征的化学方程式与它所代表的宏观事物和现象、反映的微观结构和反应机理、体现的概念和原理紧密地联系起来,形成化学方程式“宏观-微观-符号”三重表征,进而帮助学生理解化学方程式。[8]
综上所述,化学方程式的意义要从多方面来理解,如“宏观”和“微观”,“质”和“量”,化学方程式与实验现象、条件、反应类型的关系等。而中考越来越注重以上各方面的综合运用的考察,课堂上要多将化学方程式与实验相结合。
学习目标
1、知识与技能
(1)知道化学方程式是描述化学变化的语言。化学变化过程中,反应物和生成物的组成(即质的关系)、微观粒子数目关系、各物质间质量的关系、反应条件、部分反应现象、某些反应的发生装置等都可以通过化学反应方程式用简洁的语言加以描述。
(2)能从“宏观”和“微观”,“质”与“量”的角度说出化学方程式的含义,根据化学方程式列举化学反应的有关信息。
(3)能建立化学反应微观、宏观与化学方程式三重表征的联系。
2、过程与方法
(1)通过学习化学方程式,体会化学语言在化学研究中的重要作用,增强规范使用化学语言的意识。
(2)通过建立化学反应微观、宏观与化学方程式三重表征的联系,掌握用文字、图形和化学方程式多方式表述化学反应。
3、情感态度与价值观
通过从“质”和“量”的角度对化学变化的认识,初步感受化学反应中,“量”的变化是由于“质”的变化引起的,而“质”的变化又始终是在“量”的守恒中进行的。体会“变”与“不变”的矛盾和统一,增进对辩证唯物主义观点的认识,进一步丰富物质的变化观。
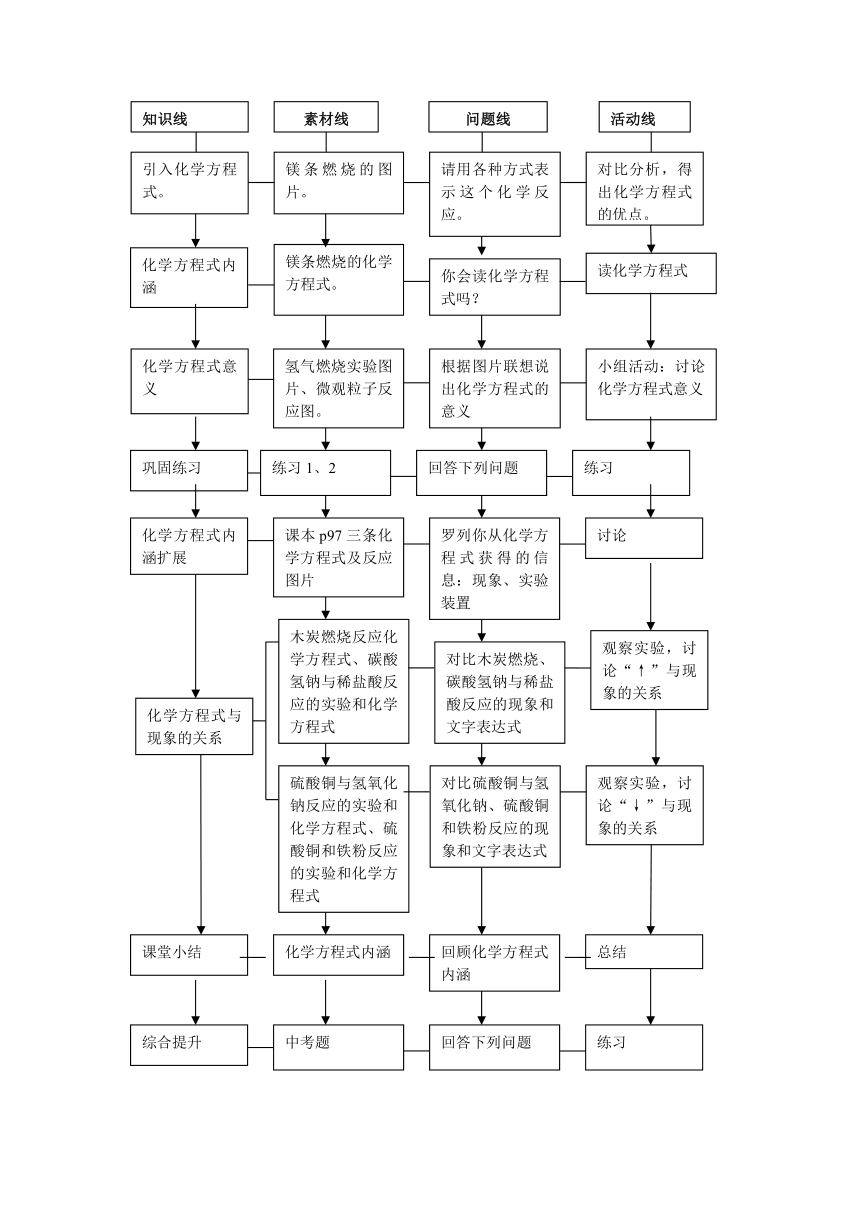
教学流程框图
教学过程设计(突出科学性)
二、化学方程式
【复习】小测:质量守恒定律
1、化学方程式概念
【讨论】展示镁条燃烧的图片,请用各种方式表示这个化学反应,看谁的更简洁,更科学。
(1)文字描述(2)文字表达式(3)符号表达式(4)化学方程式
【讨论】上述表达方式有什么优缺点?哪一种更科学?
(1)-(3)的表述文字较多,不够简洁,不能体现质量守恒定律。化学方程式更简洁且能体现质量守恒定律,更科学。
【讲述】化学方程式概念
利用化学式来表示化学反应的式子,叫做化学方程式。
2、化学方程式内涵
【读一读】你会读该反应方程式吗?2Mg+ O22MgO
【小结】化学方程式能表示化学反应的反应物、生成物和反应条件。
3、化学方程式意义
(1)展示氢气燃烧图片,结合化学方程式,用通顺规范的语言描述反应。
【讨论】从化学方程式中你可以找到以下的信息:反应物、生成物、反应条件。
(2)请从微观角度解释化学方程式的意义,再结合微观图加深理解。
【讨论】从化学方程式中可以知道:
①参加反应的原子的种类和个数是否发生变化?反应前氢原子一共多少个?氧原子一共多少个?反应后呢?是否遵守质量守恒定律?
②参加反应的分子种类和个数是否发生变化?各参加反应的分子个数比是多少?如果参加反应的氢分子有2个,则有多少个氧分子参加反应?生成多少个水分子?如果参加反应的氢分子有4个呢?如果生成10个的水分子,则参加反应的氢分子和氧分子分别有多少个?
③因此我们可以从微观角度这样描述这个化学方程式:每两个氢分子与每一个氧分子在点燃条件下生成一个水分子。
(3)回忆质量守恒定律,思考化学方程式能否体现质量守恒定律,用图片表示“=”,再用通顺规范的语言描述。
【讨论】①参加反应的各分子质量比?参加反应的各物质质量比?②如果4g氢气参加反应,则需多少的氧气?生成多少的水?如果生成18g的水呢?③因此我们可以从质量角度这样描述这个化学方程式:每4份质量的氢气与每32份质量的氧气在点燃条件下反应生成36份质量的水。
【练习】1、《学业评价》p67 1.
2、实验中反应的化学方程式为2H2O2H2↑+O2↑。B试管中
产生的气体可以使带火星的木条复燃,当B中气体的分子
数目为n时,A中气体分子数为 _______________。
4、化学方程式内涵扩展
【讨论】下列化学反应方程式能提供哪些信息?
①S+O2SO2 ②Fe+CuSO4===Cu+FeSO4 ③CuO+H2Cu+H2O
【讲述】除了“质”、“量”、“微观”三种意义,我们还应该从化学方程式中获得以下信息:①S+O2SO2的反应条件、反应物、生成物,微观意义,质量关系,反应类型等。②Fe+CuSO4===Cu+FeSO4由反应物和生成物的性质推想出完整的反应现象。③CuO+H2Cu+H2O结合氢气还原氧化铜的图片,描述反应现象,设想反应的实验装置。
5、化学方程式与现象的关系
【讨论】【实验】(1)对比和两化学方程式,结合实验分析,同样是产生二氧化碳气体,观察到现象是否一样?表示的方式是否一样?为什么?
(2)对比和两化学方程式,结合实验分析,同样是产生固体,观察到现象是否一样?表示的方式是否一样?为什么?
【小结】化学方程式用“↑”或“↓”描述产生不同于反应物状态的生产物。
“↑”表示反应物无气体,生成物生成了气体。
“↓”表示反应物无固体,生成物生成了固体沉淀。
6、小结
化学方程式的意义:(1)“质”的意义(2)“量”的意义(3)“微观”的意义
(4)反应的类型(5)反应的条件(7)反应的现象
7、课堂练习
3.实验室制取二氧化碳常使用大理石小颗粒和稀盐酸反应,反应的化学方程式为则可以观察到的实验现象是___________________________,应该选用的发生装置是________
8、布置作业 《课堂评估》
测试题组
某化学反应的微观示意图如下,图中“ ”和“ ”分别表示不同的原子。
下列说法不正确的是
A.每3g物质Ⅰ与1g物质Ⅱ恰好完全反应生成2g物质Ⅲ
B.每3个物质Ⅰ分子与1个物质Ⅱ分子恰好完全反应生成2个物质Ⅲ分子
C.每3万个物质Ⅰ分子与1万个物质Ⅱ分子恰好完全反应生成2万个物质Ⅲ分子
D.每3n个物质Ⅰ分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子
教学反思:
教学方法是以问题引导的方法引导学生归纳化学方程式的内涵,但问题不够细致,不能突出学生学习过程中出现的问题,应该把问题细致化:
①宏观意义
认真阅读化学方程式,回答下列问题
反应物是______,生成物是_______,反应条件是_____。
“+”表示______,“====”表示______
读法____________________________________________。
②微观意义
从微观粒子的角度回答下面的问题:
参加反应的微粒有__________,生成的微粒有__________。
参加反应的微粒个数比是:________________________
读法:每__________和__________在点燃的条件下生成_________。
③量的意义
从质量的角度回答下面问题:
参加反应的各分子的质量比是__________________。
参加反应的各物质的质量比是:________________________。
读法:每__________和__________在点燃的条件下生成_________。
④其他意义
(1)宏观读:
微观读:
质量读:
(2)怎样通过化学方程式推测反应的现象?
第一步:写出各物质的物理性质。
第二步:对比反应前后的各物质的物理性质的不同。
第三步:推测现象
参考文献
[1] 李南萍.广州市义务教育阶段学科学业质量评价标准(化学)[M].广州:广东教育出版社,13-14
[2] 戴光宏.化学科[A].广州市教育局教学研究室.2013年广州市初中毕业生学业考试年报[C].广州,174
[3] 戴光宏.化学科[A].广州市教育局教学研究室.2013年广州市初中毕业生学业考试年报[C].广州,177
[4] 李南萍.化学科[A].广州市教育局教学研究室.2012年广州市初中毕业生学业考试年报[C].广州,226
[5] 李南萍.化学科[A].广州市教育局教学研究室.2011年广州市初中毕业生学业考试年报[C].广州,211-212
[6]闫亚瑞,王祖浩.有关化学方程式教学研究的国内外比较与启示[J].课程与教学.教育科学研究,2006,10,43-46
[7]刘萍.初中化学方程式的教学方法例析[J].基础教育研究,2013,9,51-52
[8]王少卿,彭守义.化学方程式教学策略[J].郑州师范教育,2013,3,77-79
知识线
素材线
问题线
活动线
引入化学方程式。
化学方程式内涵
化学方程式意义
镁条燃烧的图片。
请用各种方式表示这个化学反应。
对比分析,得出化学方程式的优点。
镁条燃烧的化学方程式。
你会读化学方程式吗?
读化学方程式
氢气燃烧实验图片、微观粒子反应图。
根据图片联想说出化学方程式的意义
小组活动:讨论化学方程式意义
课本p97三条化学方程式及反应图片
综合提升
罗列你从化学方程式获得的信息:现象、实验装置
讨论
化学方程式内涵扩展
中考题
回答下列问题
练习
化学方程式与现象的关系
木炭燃烧反应化学方程式、碳酸氢钠与稀盐酸反应的实验和化学方程式
对比木炭燃烧、碳酸氢钠与稀盐酸反应的现象和文字表达式
观察实验,讨论“↑”与现象的关系
硫酸铜与氢氧化钠反应的实验和化学方程式、硫酸铜和铁粉反应的实验和化学方程式
练习1、2
回答下列问题
练习
巩固练习
对比硫酸铜与氢氧化钠、硫酸铜和铁粉反应的现象和文字表达式
观察实验,讨论“↓”与现象的关系
课堂小结
化学方程式内涵
回顾化学方程式内涵
总结
A B
物质Ⅰ分子
物质Ⅱ分子
物质Ⅲ分子
展开更多......
收起↑
 资源预览
资源预览


 资源预览
资源预览


