 资源简介
资源简介
中小学教育资源及组卷应用平台
热点题空5 平衡图像原因解释之温度、压强对平衡的影响
【高考必备知识】
1.影响化学平衡的因素
(1)若其他条件不变,改变下列条件对化学平衡的影响
改变的条件(其他条件不变) 化学平衡移动的方向
浓度 增大反应物浓度或减小生成物浓度 向正反应方向移动
减小反应物浓度或增大生成物浓度 向逆反应方向移动
压强(对有气体参加的反应) 反应前后气体体积改变 增大压强 向气体分子总数减小的方向移动
减小压强 向气体分子总数增大的方向移动
反应前后气体体积不变 改变压强 平衡不移动
温度 升高温度 向吸热反应方向移动
降低温度 向放热反应方向移动
催化剂 同等程度改变v正、v逆,平衡不移动
(2)“惰性气体”对化学平衡移动的影响
①恒温、恒容下:加入惰性气体体系总压增大,但体积不变,各反应物、生成物的浓度均未改变,故反应速率不变,V正、V逆也不变,化学平衡也不发生移动
②恒温、恒压下:加入惰性气体体积增大各反应物浓度减少反应速率减小,V正、
V逆均减小,等效于降压,故化学平衡向气体总体积增大的方向移动
2.掌握三类平衡移动图像:反应mA(g)+nB(g)pC(g)+qD(g),m+n>p+q,且ΔH>0
(1)速率—时间图——注意断点
t1时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;t2时升高温度,对任何反应,正反应和逆反应速率均增大,吸热反应的正反应速率增大较快;t3时减小压强,容器容积增大,浓度变小,正反应速率和逆反应速率均减小;t4时使用催化剂,正反应速率和逆反应速率均瞬间增大
(2)转化率(或含量)—时间图——先拐先平
甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和的反应,压强越大,反应物的转化率越大;乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,反应物的转化率越大;丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变反应物的转化率
(3恒压(温)线——定一议二
分析时可沿横轴作一条平行于纵轴的虚线,即:为等压线或等温线,然后分析另一条件变化对该反应的影响
【答题模板及剖析】
恒压线(恒温线)
答题策略 叙特点(反应特点或容器特点)→变条件→定方向→得结论(或结果)
答题模板 该反应的正反应是气体分子数减小(或增大)的反应,当温度一定时,增大压强,平衡正向移动,因此×××(得结论)
经典例题 乙烯气相水合反应的热化学方程式为C2H4(g)+H2O(g)===C2H5OH(g) ΔH=-45.5 kJ·mol-1,下图是乙烯气相水合法制乙醇中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。图中压强(p1、p2、p3、p4)的大小顺序为__________,理由是______________ INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K538.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2019赵瑊\\看PPT\\考前三个月 化学 通用\\全书完整的Word版文档\\第二篇\\K538.TIF" \* MERGEFORMATINET
标注答案 p1<p2<p3<p4,反应正方向是分子数减少的反应,相同温度下,压强升高乙烯转化率提高
【题组训练】
1.对反应:3SO2(g)+2H2O (g)===2H2SO4(l)+S(s) ΔH2=-254 kJ·mol-1,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2_______p 1(填“>”或“<”),得出该结论的理由是__________________________
2.反应Ⅱ:2H2SO4(l)===2SO2(g)+O2(g)+2H2O(g) ΔH=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)===SO3(g)+H2O(g) ΔH=+177 kJ·mol-1
ii.SO3(g)分解
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
(1)X代表的物理量是________________
(2)判断L1、L2的大小关系,并简述理由__________________________________________
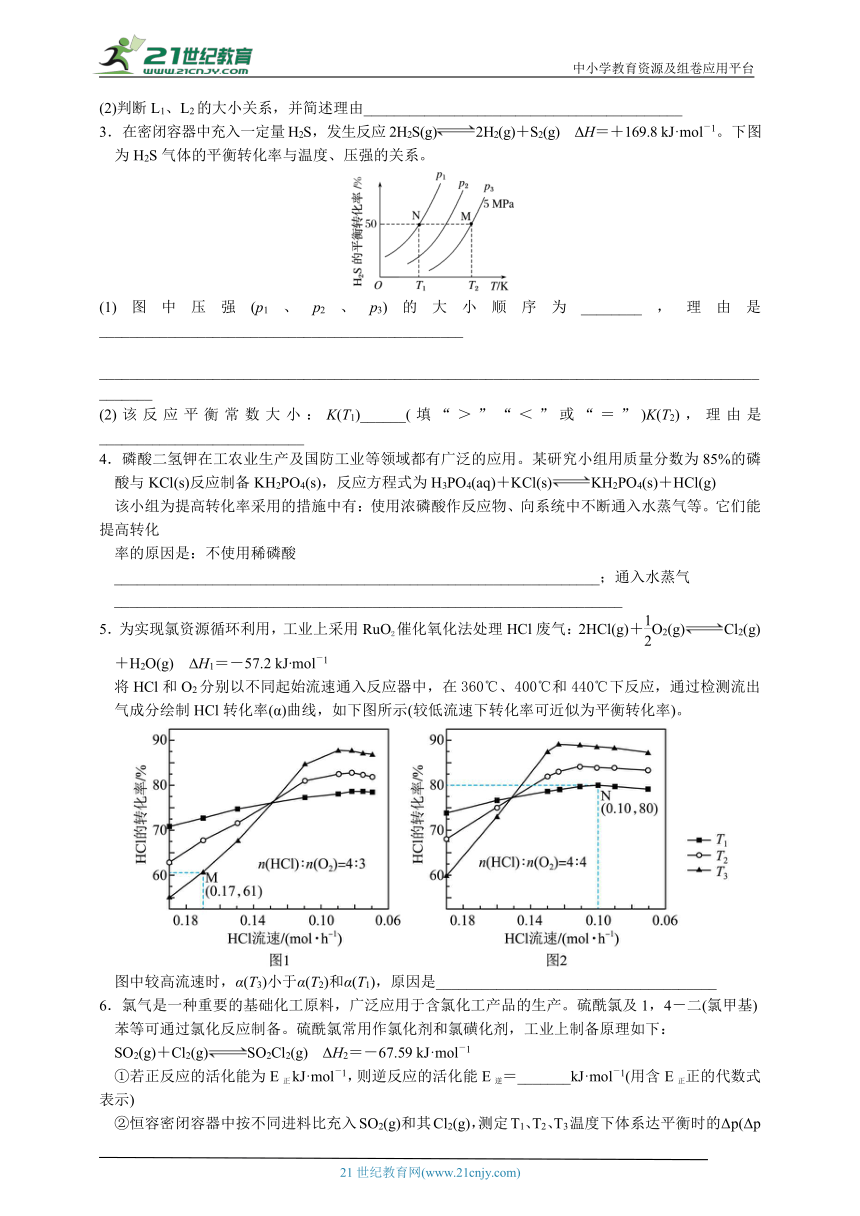
3.在密闭容器中充入一定量H2S,发生反应2H2S(g)2H2(g)+S2(g) ΔH=+169.8 kJ·mol-1。下图为H2S气体的平衡转化率与温度、压强的关系。
INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K522.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2019赵瑊\\看PPT\\考前三个月 化学 通用\\全书完整的Word版文档\\第二篇\\K522.TIF" \* MERGEFORMATINET
(1)图中压强(p1、p2、p3)的大小顺序为________,理由是________________________________________________
______________________________________________________________________________________________
(2)该反应平衡常数大小:K(T1)______(填“>”“<”或“=”)K(T2),理由是___________________________
4.磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与KCl(s)反应制备KH2PO4(s),反应方程式为H3PO4(aq)+KCl(s)KH2PO4(s)+HCl(g)
该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化
率的原因是:不使用稀磷酸________________________________________________________________;通入水蒸气___________________________________________________________________
5.为实现氯资源循环利用,工业上采用RuO2催化氧化法处理HCl废气:2HCl(g)+O2(g)Cl2(g)+H2O(g) H1=-57.2 kJ mol-1
将HCl和O2分别以不同起始流速通入反应器中,在360℃、400℃和440℃下反应,通过检测流出气成分绘制HCl转化率(α)曲线,如下图所示(较低流速下转化率可近似为平衡转化率)。
图中较高流速时,α(T3)小于α(T2)和α(T1),原因是_____________________________________
6.氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及1,4-二(氯甲基)苯等可通过氯化反应制备。硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
SO2(g)+Cl2(g)SO2Cl2(g) ΔH2=-67.59 kJ·mol-1
①若正反应的活化能为E正kJ·mol-1,则逆反应的活化能E逆=_______kJ·mol-1(用含E正正的代数式表示)
②恒容密闭容器中按不同进料比充入SO2(g)和其Cl2(g),测定T1、T2、T3温度下体系达平衡时的Δp(Δp=p0-p,p0为体系初始压强,p0=240 kPa,P为体系平衡压强),结果如图
上图中温度由高到低的顺序为_______,判断依据为_______。M点Cl2的转化率为_______,T1温度下用分压表示的平衡常数Kp=_______ kPa-1
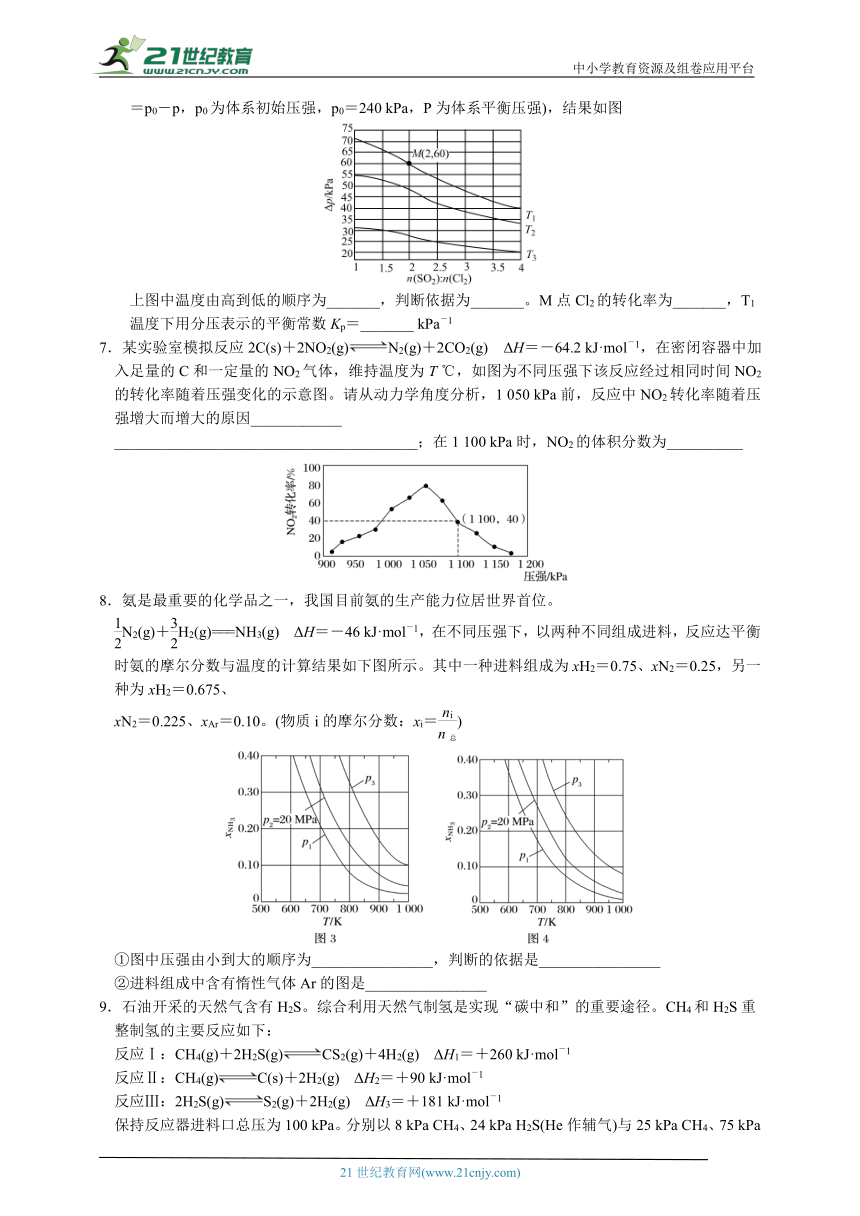
7.某实验室模拟反应2C(s)+2NO2(g)N2(g)+2CO2(g) ΔH=-64.2 kJ·mol-1,在密闭容器中加入足量的C和一定量的NO2气体,维持温度为T ℃,如图为不同压强下该反应经过相同时间NO2的转化率随着压强变化的示意图。请从动力学角度分析,1 050 kPa前,反应中NO2转化率随着压强增大而增大的原因____________
________________________________________;在1 100 kPa时,NO2的体积分数为__________
INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\调79.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\调79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\全书完整的Word版文档\\调79.TIF" \* MERGEFORMATINET
8.氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。
N2(g)+H2(g)===NH3(g) ΔH=-46 kJ·mol-1,在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为xH2=0.75、xN2=0.25,另一种为xH2=0.675、
xN2=0.225、xAr=0.10。(物质i的摩尔分数:xi=)
INCLUDEPICTURE "D:\\张彦丽\\2023年\\高考题\\化学\\G79.TIF" \* MERGEFORMAT INCLUDEPICTURE "D:\\张彦丽\\2023年\\高考题\\化学\\G79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\张彦丽\\2023年\\高考题\\化学\\G79.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\张彦丽\\2023年\\高考题\\化学\\G78.TIF" \* MERGEFORMAT INCLUDEPICTURE "D:\\张彦丽\\2023年\\高考题\\化学\\G78.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\张彦丽\\2023年\\高考题\\化学\\G78.TIF" \* MERGEFORMATINET
①图中压强由小到大的顺序为________________,判断的依据是________________
②进料组成中含有惰性气体Ar的图是________________
9.石油开采的天然气含有H2S。综合利用天然气制氢是实现“碳中和”的重要途径。CH4和H2S重整制氢的主要反应如下:
反应Ⅰ:CH4(g)+2H2S(g)CS2(g)+4H2(g) ΔH1=+260 kJ·mol-1
反应Ⅱ:CH4(g)C(s)+2H2(g) ΔH2=+90 kJ·mol-1
反应Ⅲ:2H2S(g)S2(g)+2H2(g) ΔH3=+181 kJ·mol-1
保持反应器进料口总压为100 kPa。分别以8 kPa CH4、24 kPa H2S(He作辅气)与25 kPa CH4、75 kPa H2S进料。CH4平衡转化率与温度的关系如图1,含有He的曲线为 _______,理由是 ___________________
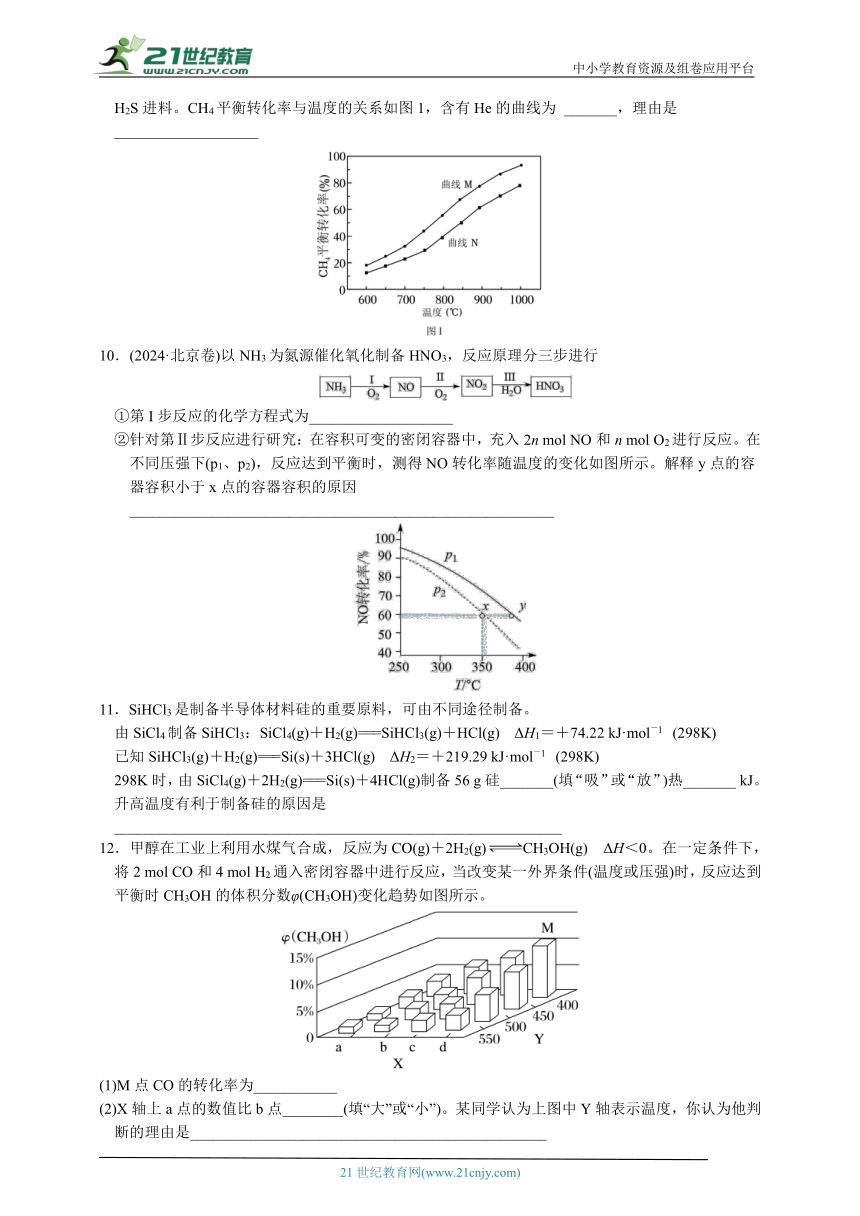
10.(2024·北京卷)以NH3为氮源催化氧化制备HNO3,反应原理分三步进行
①第I步反应的化学方程式为___________________
②针对第Ⅱ步反应进行研究:在容积可变的密闭容器中,充入2n mol NO和n mol O2进行反应。在不同压强下(p1、p2),反应达到平衡时,测得NO转化率随温度的变化如图所示。解释y点的容器容积小于x点的容器容积的原因________________________________________________________
11.SiHCl3是制备半导体材料硅的重要原料,可由不同途径制备。
由SiCl4制备SiHCl3:SiCl4(g)+H2(g)===SiHCl3(g)+HCl(g) ΔH1=+74.22 kJ·mol-1 (298K)
已知SiHCl3(g)+H2(g)===Si(s)+3HCl(g) ΔH2=+219.29 kJ·mol-1 (298K)
298K时,由SiCl4(g)+2H2(g)===Si(s)+4HCl(g)制备56 g硅_______(填“吸”或“放”)热_______ kJ。升高温度有利于制备硅的原因是___________________________________________________________
12.甲醇在工业上利用水煤气合成,反应为CO(g)+2H2(g)CH3OH(g) ΔH<0。在一定条件下,将2 mol CO和4 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,反应达到平衡时CH3OH的体积分数φ(CH3OH)变化趋势如图所示。
INCLUDEPICTURE "E:\\靖春春\\2022\\大二轮\\化学 江苏专用 新高考\\doc\\X648.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\靖春春\\2022\\大二轮\\化学 江苏专用 新高考\\doc\\X648.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\靖春春\\2022\\大二轮\\化学 江苏专用 新高考\\doc\\X648.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\靖春春\\2022\\大二轮\\化学 江苏专用 新高考\\word\\doc\\X648.TIF" \* MERGEFORMATINET
(1)M点CO的转化率为___________
(2)X轴上a点的数值比b点________(填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_______________________________________________
13.在一定条件下,向恒容密闭容器中充入1.0 mol CO2和3.0 mol H2,在一定温度范围内发生如下转化:
CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH=-x kJ·mol-1 (x>0)。在不同催化剂作用下,相同时间内CO2的转化率随温度的变化如图所示:
INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\333.TIF" \* MERGEFORMAT INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\第一部分\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\第一部分\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\第一部分\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "D:\\2022唐兰\\二轮\\大二轮\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\第一部分\\333.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张潇\\2022\\二轮\\看PPT\\化学 大二轮 新教材 老高考(黑吉晋皖云)\\教师用书Word版文档\\第一部分 二轮专题突破\\333.TIF" \* MERGEFORMATINET
(1)催化效果最佳的是催化剂______(填“Ⅰ”“Ⅱ”或“Ⅲ”);b点v正______(填“>”“<”或“=”)v逆
(2)此反应在a点时已达到平衡状态,a点的转化率比c点高的原因是_____________________
14.乙苯催化脱氢制苯乙烯反应: ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实_____________________________________
INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K528.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2019赵瑊\\看PPT\\考前三个月 化学 通用\\全书完整的Word版文档\\第二篇\\K528.TIF" \* MERGEFORMATINET
15.已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g) ΔH<0,图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=,n(CO2))
(1)图1中投料比相同,温度从高到低的顺序为____________________,判断依据是______________________
_____________________________________________________________________________________________
(2)图2中m1、m2、m3从大到小的顺序为____________,判断依据是_________________________________
INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K529.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2019赵瑊\\看PPT\\考前三个月 化学 通用\\全书完整的Word版文档\\第二篇\\K529.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K530.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2019赵瑊\\看PPT\\考前三个月 化学 通用\\全书完整的Word版文档\\第二篇\\K530.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K531.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\WORD\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\张红\\2019\\大二轮\\考前三个 化学通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\2019赵瑊\\看PPT\\考前三个月 化学 通用\\全书完整的Word版文档\\第二篇\\K531.TIF" \* MERGEFORMATINET
16.甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:ⅰ、CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1=-63kJ·mol-1
ⅱ、CO2(g)+H2(g)CO(g)+H2O(g) ΔH2==+36 kJ·mol-1
ⅲ、CH3OH(g)CO(g)+2H2(g) ΔH3=+99 kJ·mol-1
一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。温度为470 K时,图中P点________(填“是”或“不是”)处于平衡状态。在490 K之前,甲醇产率随着温度升高而增大的原因是__________________________________________________________________;
490 K之后,甲醇产率下降的原因是_________________________________________________________________
17.容积均为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g)N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是______________________________________________
INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\165.TIF" \* MERGEFORMAT INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\word\\165.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2019\\二轮\\化学\\化学 人教通用\\全书完整的Word版文档\\165.TIF" \* MERGEFORMATINET
18.实验测定2H2S(g)2H2(g)+S2(g) ΔH=+169.8 kJ·mol-1的化学平衡常数Kp随温度变化的曲线是如图中的________(填“a”或“b”),理由是_____________________________________________
【热点题空5 平衡图像原因解释之温度、压强对平衡的影响】答案
1.> 反应Ⅱ是气体物质的量减小的反应,温度一定时,增大压强使反应正向移动,H2SO4 的物质的量增大,体系总物质的量减小,H2SO4的物质的量分数增大
2.(1)压强
(2)L2>L1 2SO3(g)===2SO2(g)+O2(g) ΔH=+196 kJ·mol-1,压强一定时,温度升高,平衡转化率增大
3.(1)p1<p2<p3 该反应的正反应是气体分子数增大的反应,其他条件不变时,减小压强使平衡正向移动,H2S的平衡转化率增大,由图像上看,相同温度,p1条件下H2S的平衡转化率最大,p3条件下H2S的平衡转化率最小
(2)< 该反应正向是吸热反应,升高温度,平衡正向移动,平衡常数增大
4.使用浓磷酸作反应物可以提高磷酸的浓度,促使反应正向进行
使得气体中氯化氢的分压减小,促使反应正向进行
解析:使用浓磷酸作反应物可以提高磷酸的浓度,促使反应正向进行;向系统中不断通入水蒸气,使得气体中氯化氢的分压减小,促使反应正向进行;都可以促进氯化钾的转化率的提高;
5.反应未达到平衡,T3温度低,反应速率慢,相同时间内HCl的转化率低
解析:图中较高流速时,反应未达到平衡状态,T3温度低,反应速率慢,故HCl的转化率低;
6.①E正+67.59
②T3>T2>T1 Δp与生成的SO2Cl2的压强相等,该反应放热,升温平衡逆向移动,生成的SO2Cl2的量减少, Δp减小 75% 0.03
解析:①ΔH=正反应的活化能-逆反应的活化能。代入数据得:-67.59 kJ·mol-1=E正kJ·mol-1-E逆,则E逆=(E正+ 67.59)kJ·mol-1。②该反应为气体分子数减小的反应,由反应方程式可知,恒温恒容条件下,体系达平衡时,体系中减小的压强等于生成的SO2Cl2的压强,该反应为放热反应,升高温度,平衡逆向移动,生成的SO2Cl2的量减少,则Δp减小,对照图像可知T1 SO2(g)+Cl2(g)SO2Cl2(g)
起始/kPa 160 80 0
转化/kPa x x x
平衡/kPa 160-x 80-x x
由图可知,M点处Δp=p0-p=60 kPa,将p0=240 kPa、p=(160-x+80-x+x)kPa代入,解得x=60,则M点Cl2的转化率为×100%=75%。T1温度下平衡时各气体分压分别为p(SO2)=100 kPa,p(Cl2)=20 kPa,p(SO2Cl2)=60 kPa,代入平衡常数表达式:Kp===0.03 kPa-1。③体系初始压强相同,当n(SO2)∶n(Cl2)<1.0时,随着进料比n(SO2)∶n(Cl2)增大,生成的SO2Cl2的量增多, Δp增大,按化学计量数之比投料时,产物的产率最高,当n(SO2)∶n(Cl2)>1.0时,随着进料比n(SO2)∶n(Cl2)增大,Δp减小,排除A、B;结合②中计算可知,当n(SO2)∶n(Cl2)=0.5时,体系中生成的SO2Cl2的分压也为60 kPa,即Δp=60 kPa,对照图像可知,表示T1温度下Δp随进料比变化的是D。
7.1 050 kPa前反应未达平衡状态,随着压强增大,反应速率加快,NO2转化率提高 50%
解析:根据示意图,1 050 kPa前,反应未达到平衡,随着压强增大,反应速率增大,NO2的转化率加快;假设通入1 mol NO2,
2C(s)+2NO2(g)N2(g)+2CO2(g)
起始/mol 1 0 0
变化/mol 0.4 0.2 0.4
平衡/mol 0.6 0.2 0.4
1 100 kPa时,NO2的体积分数为×100%=50%。
8.①p1<p2<p3 合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分数越大
②图4
解析:①合成氨的反应中,压强越大越有利于氨的合成,因此,压强越大平衡时氨的摩尔分数越大。由图中信息可知,在相同温度下,反应达平衡时氨的摩尔分数p1<p2<p3,因此,图中压强由小到大的顺序为p1<p2<p3。②该反应为气体分子数减少的反应,在相同温度和相同压强下,惰性气体Ar不利于合成氨,进料组成中含有惰性气体Ar的图是图4。③图3中,进料组成为xH2=0.75、xN2=0.25,两者物质的量之比为3∶1。假设进料中氢气和氮气的物质的量分别为3 mol和1 mol,达到平衡时氮气的变化量为x mol,则有:
N2(g)+3H2(g)2NH3(g)
始/mol 1 3 0
变/mol x 3x 2x
平/mol 1-x 3-3x 2x
当p2=20 MPa、xNH3=0.20时,xNH3==0.20,解得x=,则氮气的转化率α=≈33.33%,平衡时N2、H2、NH3的物质的量分别为 mol、2 mol、 mol,其物质的量分数分别为、、,则该温度下K==(MPa)-2,因此,该温度时反应N2(g)+H2(g)NH3(g)的平衡常数Kp===(MPa)-1。
9.M 总压一定,充入氦气,反应物分压减小,相当于减压,反应Ⅰ、Ⅱ均正向移动,CH4平衡转化率增大
解析:保持反应器进料口总压为100kPa。分别以8 kPa CH4、24 kPa H2S(He作辅气)与25 kPa CH4、75 kPa H2S进料。CH4平衡转化率与温度的关系如图1,含有He的曲线为M,理由是总压一定,充入氦气,反应物分压减小,相当于减压,反应Ⅰ、Ⅱ均正向移动,CH4平衡转化率增大
10.①4NH3+5O24NO+6H2O
②2NO+O22NO2,该反应正反应气体分子数减少,同温时,p1条件下NO转化率高于p2,故p1>p2,x、y点转化率相同,气体总物质的量相同,此时压强对容积的影响大于温度对容积的影响
解析:①第Ⅰ步反应为氨气的催化氧化,化学方程式为4NH3+5O24NO+6H2O;②第Ⅱ步反应为2NO+O22NO2,该反应正反应气体分子数减少,同温时,p1条件下NO转化率高于p2,故p1>p2,x、y点转化率相同,则气体总物质的量n相同,根据V=nR,升温体积增大,加压体积减小,此时压强对容积的影响大于温度对容积的影响,故y点的容器容积小于x点的容器容积。
11.吸 587.02 该反应为吸热反应,升高温度,反应正向移动,有利于制备硅
解析:(1)由题给热化学方程式:①SiCl4(g)+H2(g)===SiHCl3(g)+HCl(g) ΔH1=+74.22 kJ·mol-1;
②SiHCl3(g)+H2(g)===Si(s)+3HCl(g) ΔH2=+219.29 kJ·mol-1;则根据盖斯定律可知,①+②,可得热化学方程式SiCl4(g)+2H2(g)===Si(s)+4HCl(g),ΔH=ΔH1+ΔH2=+74.22 kJ·mol-1+(+219.29 kJ·mol-1)=+293.51
kJ·mol-1,则制备56 g Si,即2 mol Si,需要吸收热量为293.51 kJ·mol-1×2=587.02 kJ·mol-1;该反应为吸热反应,升高温度,反应正向移动,有利于制备硅。
12.(1)25%
(2)小 该反应正反应是放热反应,温度降低,平衡正向移动,φ(CH3OH)增大
13.(1)Ⅰ > (2)该反应为放热反应,升高温度,平衡逆向移动
解析:(1)根据图示可知,相同温度时,在催化剂Ⅰ的作用下,反应相同时间内CO2的转化率最大,因此催化剂Ⅰ的效果最好;b点时反应还未达到平衡状态,CO2的转化率还会继续增大,反应正向进行,因此v正>v逆。(2)该反应为放热反应,a点时达到平衡,从a点到c点,温度升高,平衡逆向移动,CO2的转化率下降。
14.正反应方向气体分子数增加,压强不变,加入水蒸气相当于起减压的效果,使平衡正向移动,乙苯的平衡转化率增大
15.(1)T3>T2>T1
正反应放热,升高温度平衡逆向移动,温度越高,CO2的平衡转化率越小,所以T3>T2>T1
(2)m1>m2>m3 保持n(CO2)不变,增大n(H2),平衡正向移动,CO2的平衡转化率增大,所以m1>m2>m3
16.不是 温度越高化学反应速率越快;升高温度,反应ⅰ逆向移动、催化剂活性降低
解析:温度为470 K时,图中P点不是处于平衡状态。在490 K之前,甲醇产率随着温度升高而增大的原因是温度越高化学反应速率越快;490 K之后,甲醇产率下降的原因是升高温度,反应ⅰ逆向移动、催化剂活性降低
17.0~3 s内温度升高对速率的影响大于浓度降低的影响
18.a 正反应为吸热反应,升高温度,平衡常数增大,负对数减小,曲线a满足
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
展开更多......
收起↑
 资源预览
资源预览


 资源预览
资源预览




