 资源简介
资源简介
第五单元 化学反应的定量关系 单元提升卷
时间:60分钟 满分:60分
可能用到的相对原子质量:
一、选择题(本大题共10小题,每小题2分,共20分。在每小题给出的四个选项中,只有一项符合题目要求)
1.下列现象不能用质量守恒定律解释的是( )
A. 盐溶于水中得到的盐水
B. 镁在氧气中完全燃烧生成氧化镁
C. 木材在空气中燃烧后化为灰烬,灰烬的质量比木材的小
D. 铜丝在空气中加热,生成物的质量比原来铜丝的质量大
2.利用空间站微重力环境进行材料的加工与生产是空间站的重要应用,如制备砷化镓的生产成本只有地球上的。制取砷化镓的反应为,该反应中的值是( )
A. 4 B. 3 C. 2 D. 1
3.我国新一代运载火箭采用的是低温推进剂——液氢、液氧,如长征五号火箭,反应的化学方程式为。下列从该化学方程式中获取的信息不正确的是( )
A. 在化学反应前后,元素的种类没有改变
B. 氢气与氧气在点燃的条件下反应生成水
C. 氢气与氧气充分反应生成水
D. 该反应说明水是由氢元素和氧元素组成的
4.下列化学方程式书写完全正确的是( )
A. B.
C. D.
5.小荣设计了如图所示三个实验来验证质量守恒定律,实验结束后,②中天平不平衡,其余天平均平衡(忽略气球浮力),下列有关说法正确的是( )
A. 能直接验证质量守恒定律的是①③
B. 实验①中气球先变瘪,后胀大
C. 实验②不遵守质量守恒定律
D. 将实验②中烧杯换成密封装置,实验结束,天平平衡
6.在化学反应中,已知C和D的相对分子质量之比是,当与足量A完全反应后,生成。则在此反应中,B和C的质量比是( )
A. B. C. D.
7.科研人员利用催化剂,将两种温室气体进行转化,为“碳中和”提供了一种新的途径。其反应原理如图所示,下列说法不正确的是( )
A. 该反应前后一共有两种氧化物
B. 参加反应的甲与丁的质量比为
C. 乙和丁中碳元素的化合价相同
D. 参加反应的甲与乙的分子个数比为
8.将下列四种物质放入密闭容器中充分反应,测得反应前后各物质的质量如表。下列说法不正确的是( )
物质 甲 乙 丙 丁
反应前的质量/ 30 20 5 0
反应后的质量/ 14 16 20
A.
B. 丁一定是化合物
C. 丙可能是催化剂
D. 参加反应的甲和生成的丁的质量比为
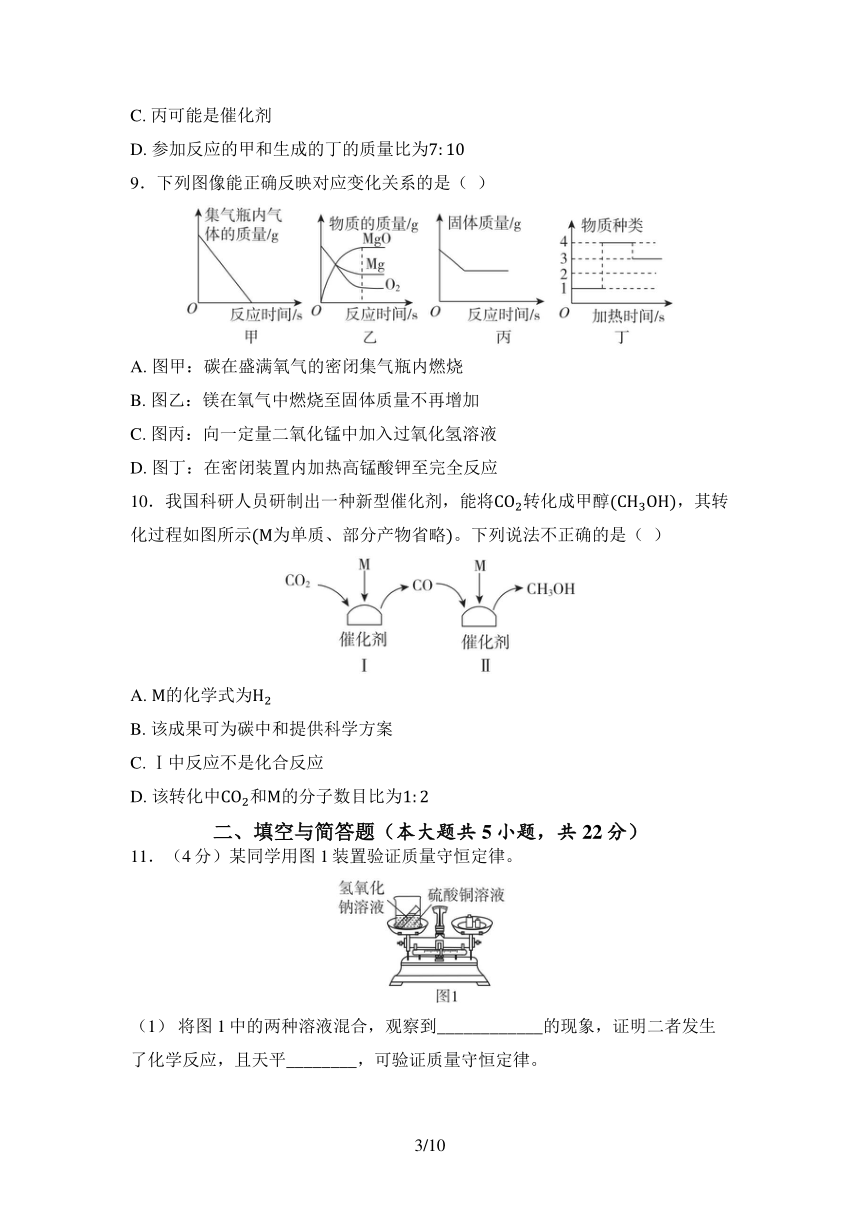
9.下列图像能正确反映对应变化关系的是( )
A. 图甲:碳在盛满氧气的密闭集气瓶内燃烧
B. 图乙:镁在氧气中燃烧至固体质量不再增加
C. 图丙:向一定量二氧化锰中加入过氧化氢溶液
D. 图丁:在密闭装置内加热高锰酸钾至完全反应
10.我国科研人员研制出一种新型催化剂,能将转化成甲醇,其转化过程如图所示为单质、部分产物省略。下列说法不正确的是( )
A. 的化学式为
B. 该成果可为碳中和提供科学方案
C. Ⅰ中反应不是化合反应
D. 该转化中和的分子数目比为
二、填空与简答题(本大题共5小题,共22分)
11.(4分)某同学用图1装置验证质量守恒定律。
(1) 将图1中的两种溶液混合,观察到_ _ _ _ _ _ _ _ _ _ _ _ 的现象,证明二者发生了化学反应,且天平_ _ _ _ _ _ _ _ ,可验证质量守恒定律。
(2) 仅利用图1中的仪器,可继续验证质量守恒定律的实验是_ _ _ _ (填字母)。
A. 冰融化成水
B. 铁钉和硫酸铜溶液反应
C. 碳酸钙固体和稀盐酸混合
(3) 该同学以电解水为例,用图2从分子和原子的角度解释质量守恒定律的微观本质,请你帮他补充完整。
12.(5分)配平下列化学方程式。
(1) _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(2) _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(3) _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(4) _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(5) _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
13.(4分)我国科学家在水煤气变换中引入了双催化剂体系,使该反应可在时进行,反应过程如图所示。
(1) 该反应过程中不变的是_ _ (填“原子”或“分子”)。
(2) 分析整个过程,写出水煤气变换反应的化学方程式:_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(3) 参加反应的甲和丙的质量比为_ _ _ _ _ _ _ _ (填最简整数比)。
(4) 你对催化剂的新认识是_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ (写一条)。
14.(5分)质量守恒定律的发现,使得化学科学由定性研究走向定量研究,促进了化学科学的发展。
(1) 银锌纽扣电池的反应原理是,的化学式为_ _ _ _ _ _ _ _ _ _ _ _ ,_ _ (填“是”或“不是”)氧化物。
(2) 高锰酸钾中含有氧元素的质量为,则加热高锰酸钾至完全分解,理论上可以得到氧气的质量_ _ (填“大于”“等于”或“小于”)。
(3) “中国芯”的主要材料是高纯度的单质硅,工业上可用和碳单质在高温条件下反应来制取硅,该反应同时生成气体,化学方程式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(4) 尿素是一种农业上常用的高效氮肥。在高温、高压条件下二氧化碳和氨气反应生成尿素和水,化学方程式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
15.(4分)工业上以钛铁矿主要成分为钛酸亚铁,还含有少量、等为原料制金属钛的工艺流程如下:
已知:钛、镁在高温下与空气中的氧气、二氧化碳等反应。
(1) 硫酸氧钛中钛元素的化合价为_ _ _ _ _ _ ;钛铁矿中的和硫酸反应可生成硫酸铁和水,其化学方程式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(2) 工业上常在高温和氩气氛围中,用金属镁和反应的方法制备,氩气的作用是_ _ _ _ (填字母)。
A. 催化剂 B. 保护气 C. 反应物
(3) 可与焦炭、氯气在高温下反应,该反应中氯气和碳按质量比参加反应,则化学方程式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
三、实验与探究题(本大题共2小题,共13分)
16.(6分)老师组织同学们对质量守恒定律进行实验探究。回答相关问题。
(1) 第1小组设计的实验方案如图1所示,用电子天平称量加入盐酸前后整个装置的质量。加入盐酸后,锥形瓶中发生反应的化学方程式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ ,比较读数发现反应前后的质量并不相等,其原因是_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(2) 第2小组设计了图2方案,以解决第1小组遇到的问题。但有同学认为会产生误差,他的理由是气球膨胀后不可忽略_ _ 的影响。
(3) 第3小组善于创新,设计了图3方案,既可以达到本来的实验目的,还可以测定空气中氧气的含量。
① 连接好装置后,打开弹簧夹,推或拉注射器的活塞,松开手后活塞回到原位,说明气密性_ _ (填“良好”或“不好”)。
② 关闭弹簧夹,记录注射器初始读数,利用强光引燃白磷,待白磷熄灭并冷却至室温后打开弹簧夹。为保证锥形瓶内氧气完全反应,实验应采取的措施是_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ (任答1点);想要测定空气中氧气的含量,实验中需要测定的数据是锥形瓶(含导管)的容积、_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
17.(7分)蔗糖是一种生活中常见的物质,某兴趣小组对“蔗糖的组成”进行了探究。
【作出猜想】小组同学根据学过的光合作用的知识推测,蔗糖中可能含有碳、氢、氧元素。
【实验验证】
方案一:小荣取蔗糖在空气中点燃,检验生成物中有水和二氧化碳,得出蔗糖由碳、氢、氧三种元素组成。
(1) 小德认为该方案_ _ _ _ _ _ (填“合理”或“不合理”),理由是_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
方案二:小德利用如图所示装置再次证明。实验开始前先通一会儿氮气,然后关闭弹簧夹,再点燃酒精灯加热。
(2) 先通一会儿氮气的目的是_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
(3) 若观察到小烧杯内壁有水雾出现(经测定生成气体中只含有水),说明样品中一定含有_ _ _ _ 元素。
(4) 实验结束后观察到硬质玻璃管内残留有黑色固体,经证明该黑色固体是碳单质。利用上图所示装置,另选试剂进行了验证碳单质的实验。实验过程和现象如表:
实验过程 实验现象
先在烧杯中加入足量澄清石灰水,再向管内通入氧气,点燃酒精灯 ①硬质玻璃管中的黑色固体剧烈燃烧,发出白光; ②澄清石灰水变浑浊
上述实验中①的化学方程式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
【实验结论】蔗糖由碳、氢、氧三种元素组成。
【计算验证】
(5) 事先称得方案二中玻璃管的质量为,取用蔗糖的质量为,实验结束后称得玻璃管和剩余黑色固体的总质量为。已知蔗糖分子的相对分子质量为342,则碳单质的质量为_ _ ,蔗糖分子的化学式为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 。
四、计算应用题(本大题共1小题,共5分)
18.(5分)某化学兴趣小组的同学为测定实验室里一瓶体积为的溶液中的质量,用量筒量取该溶液进行了相关实验,实验数据记录如下,请计算:
溶液固液残留物
(1) 生成氧气_ _ 。
(2) 原过氧化氢溶液中的质量(写出计算过程)。
答案
1.【答案】A
2.【答案】B
3.【答案】C
4.【答案】D
5.【答案】D
6.【答案】C
7.【答案】C
8.【答案】D
9.【答案】D
10.【答案】D
【解析】点拨:生成物甲醇中含有碳、氢、氧三种元素,反应物二氧化碳中含有碳、氧两种元素,根据质量守恒定律,则中一定含有氢元素,而反应物为单质,则为,总反应为,故该转化中和的分子数目比为,错误。
11.【答案】(1) 产生蓝色沉淀;保持平衡
(2) B
(3)
12.【答案】(1) 1;3;2;3
(2) 2;2;2;1
(3) 3;2;1;6
(4) 4;5;4;6
(5) 4;4;2;3
13.【答案】(1) 原子
(2)
(3)
(4) 在一个化学反应中可能有多个催化剂(合理即可)
14.【答案】(1) ;不是
(2) 小于
(3)
(4)
15.【答案】(1) ;
(2) B
(3)
16.【答案】(1) ;反应生成的二氧化碳逸出装置
(2) 浮力
(3) ① 良好
② 白磷足量(合理即可);反应前后注射器活塞所对应的刻度值
17.【答案】(1) 不合理;蔗糖燃烧有氧气参与,因此不能确定蔗糖中是否含有氧元素
(2) 排尽装置中的空气
(3) 氢、氧
(4)
(5) 2.4;
18.【答案】(1) 1.6
(2) 解:设过氧化氢溶液中的质量为。
则原过氧化氢溶液中的质量为
答:原过氧化氢溶液中的质量为。
/
展开更多......
收起↑
 资源预览
资源预览




 资源预览
资源预览




