 资源简介
资源简介
2025年四川省泸州市合江马街中学中考化学二模试卷
1.本试卷分为第一部分(选择题)和第二部分(非选择题)两部分。
2.第一部分满分24分,第二部分满分41分,50分钟完成,满分65分。
3.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并在规定位置粘贴考试用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试题卷上无效。考试结束后,将答题卡和试题卷交回。预祝各位考生考试顺利!
4.可能用到的相对原子质量:H—1 C—12 N—14 O—16 Ca—40 Cu—64
第一部分选择题(共24分)
一、选择题(本题共8个小题,每小题3分,只有一个选项符合题目要求。共24分)
1.人类社会的发展离不开能源。下列能源开发利用过程中通过化学变化实现化学能转变成电能的是
A.水力发电 B.风力发电 C.燃料电池发电 D.太阳能发电
2.水是生命之源,人类的生活、生产都离不开水。下列说法错误的是
A.如图是国家节水标志 B.煮沸可以降低水的硬度
C.长期饮用蒸馏水更有利于人体健康 D.工农业污染和生活污染是水体污染的主要来源
3.从分子的角度分析,下列解释错误的是
A.吹胀气球——气体分子间的间隔变大
B.缉毒犬能根据气味发现毒品——分子在不断地运动
C.液氧和氧气都能助燃——同种分子化学性质相同
D.水电解生成氢气和氧气——分子分成原子,原子重新结合成分子
4.观察实验现象是必备的化学素养,以下实验现象说法不正确的是
A.点燃氢气——产生淡蓝色火焰
B.电解水实验——正极与负极液面下降的高度相同
C.吹灭燃烧蜡烛——灯芯处产生白烟
D.加热硫酸铜晶体——固体颜色由蓝色变为白色
5.锂电池应用广泛。锂在元素周期表中的信息和锂原子的结构示意图如图所示。下列叙述正确的是
A.锂的原子序数为3
B.锂的相对原子质量为6.941g
C.锂原子中的核外电子数为1
D.锂原子在化学反应中容易得到电子
6.尿素是一种优良的氮肥,其化学式为 CO (NH2)2。下列说法错误的是
A.尿素的相对分子质量是60
B.尿素中碳元素与氢元素的质量之比是6:1
C.尿素中氮元素的质量分数约为46.7%
D.尿素能使植物枝繁叶茂、叶色浓绿
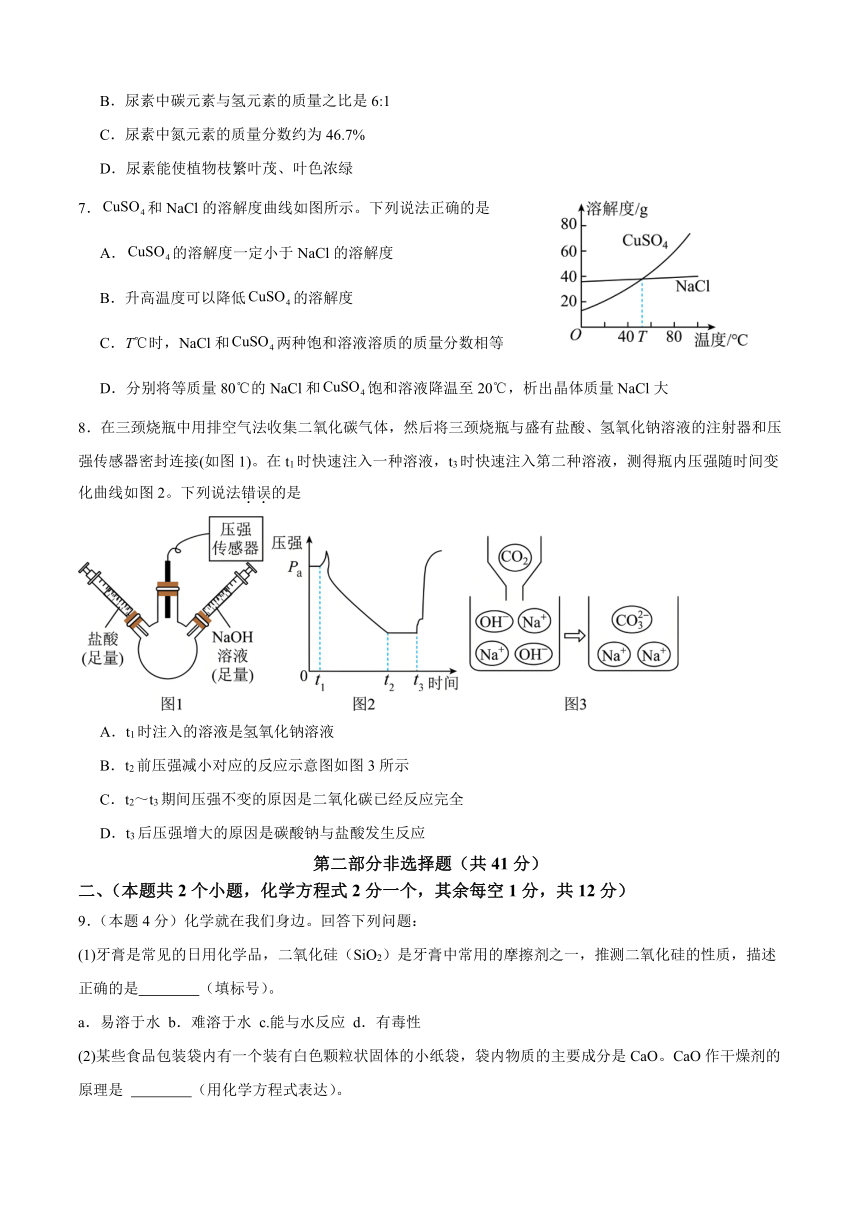
7.和NaCl的溶解度曲线如图所示。下列说法正确的是
A.的溶解度一定小于NaCl的溶解度
B.升高温度可以降低的溶解度
C.T℃时,NaCl和两种饱和溶液溶质的质量分数相等
D.分别将等质量80℃的NaCl和饱和溶液降温至20℃,析出晶体质量NaCl大
8.在三颈烧瓶中用排空气法收集二氧化碳气体,然后将三颈烧瓶与盛有盐酸、氢氧化钠溶液的注射器和压强传感器密封连接(如图1)。在t1时快速注入一种溶液,t3时快速注入第二种溶液,测得瓶内压强随时间变化曲线如图2。下列说法错误的是
A.t1时注入的溶液是氢氧化钠溶液
B.t2前压强减小对应的反应示意图如图3所示
C.t2~t3期间压强不变的原因是二氧化碳已经反应完全
D.t3后压强增大的原因是碳酸钠与盐酸发生反应
第二部分非选择题(共41分)
二、(本题共2个小题,化学方程式2分一个,其余每空1分,共12分)
9.(本题4分)化学就在我们身边。回答下列问题:
(1)牙膏是常见的日用化学品,二氧化硅(SiO2)是牙膏中常用的摩擦剂之一,推测二氧化硅的性质,描述正确的是 (填标号)。
a.易溶于水 b.难溶于水 c.能与水反应 d.有毒性
(2)某些食品包装袋内有一个装有白色颗粒状固体的小纸袋,袋内物质的主要成分是CaO。CaO作干燥剂的原理是 (用化学方程式表达)。
(3)草木灰是一种农家肥料,它的主要成分是一种含钾的盐。取一些草木灰,用水浸泡,过滤,向滤液中加入稀盐酸,生成可使澄清石灰水变浑浊的气体,由此可推断草木灰的主要成分可能是 .
10.(本题8分)水在自然界、生产和生活中都有广泛用途。
(1)硬水和软水常用 来区分;软化硬水的方法很多,在日常生活中常用 法。
(2)在水的净化过程中,常利用 (填物质名称)的吸附性除去水中异味。高铁酸钾(化学式K2FeO4)是一种新型净水剂,可用于自来水净化处理,高铁酸钾中铁元素的化合价为 价。
(3)水是重要的溶剂,配制2%的氯化钠溶液500g,不需要使用的仪器是 。(填写字母代号)
A、酒精灯 B、玻璃棒 C、烧杯 D、量筒 E、托盘天平
(4)除去NaOH溶液中混有的少量Na2CO3杂质,需加入适量的 溶液至不再产生沉淀为止,然后过滤。将滤液 ,得到NaOH固体。
(5)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO,一段时间后得到同温度的溶液乙;甲、乙溶液中溶质质量甲 乙(填“>、<、=”)。
三、(本题共2个小题,化学方程式2分一个,其余每空1分,共13分)
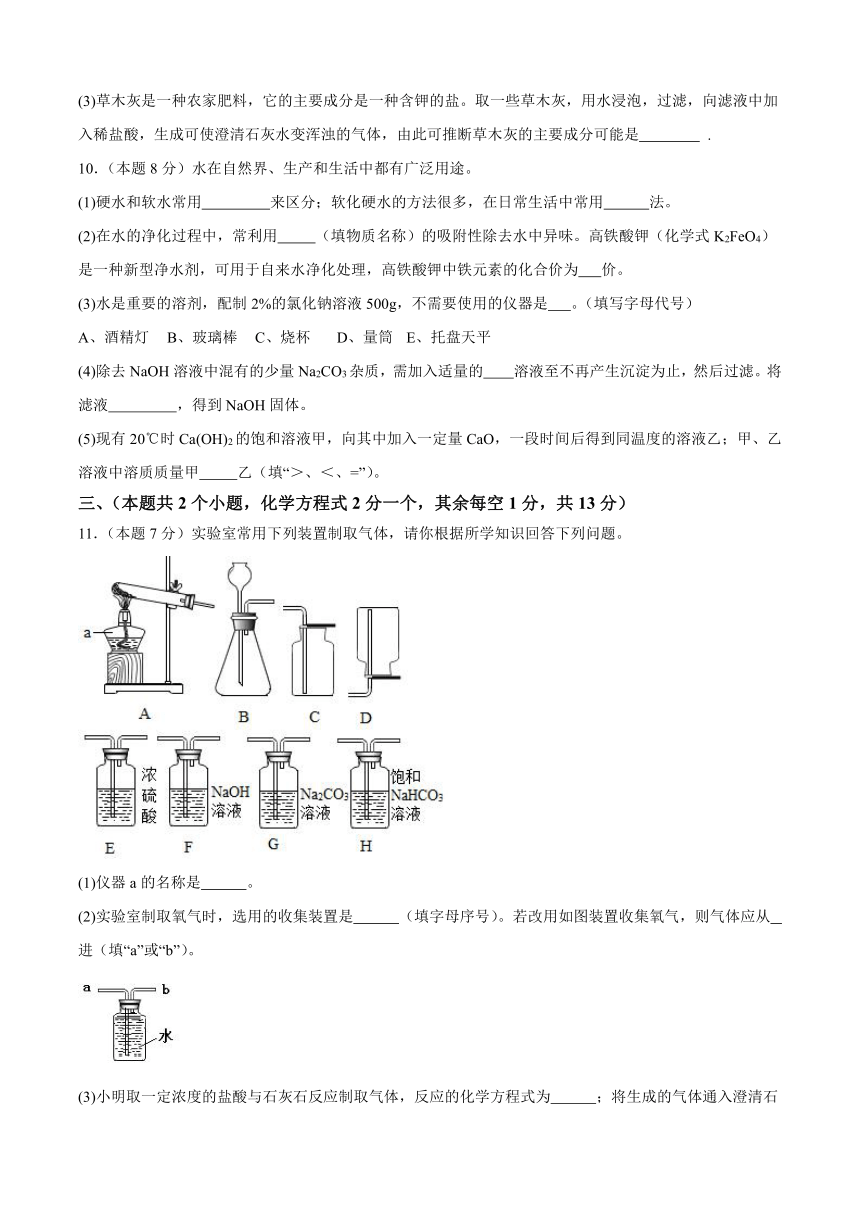
11.(本题7分)实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
(1)仪器a的名称是 。
(2)实验室制取氧气时,选用的收集装置是 (填字母序号)。若改用如图装置收集氧气,则气体应从 进(填“a”或“b”)。
(3)小明取一定浓度的盐酸与石灰石反应制取气体,反应的化学方程式为 ;将生成的气体通入澄清石灰水中,未见变浑浊。为探究其原因,进行了如下过程:
【作出猜想】石灰水已经完全变质;
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液不变色。猜想是正确,理由是 。
②如果用上述原料制得纯净、干燥的二氧化碳气体,所选仪器的连接顺序为 (填字母)。
12.(本题6分)实验室提供以下常用仪器,供完成下列气体制取实验时选用(不可重复选用)。
(1)过氧化氢(H2O2)俗称双氧水,常温下是一种无色液体,它在土豆块的催化作用下能迅速分解,放出氧气。若实验室采用该反应原理制取O2,并且在实验过程中可以随时添加双氧水,上述仪器中必需使用的有 (填序号)。该反应化学方程式为 。
(2)若使用如图所示装置充满水收集O2,则O2由 口进入;该装置除收集气体外,还可以在下列 (填序号)情况中运用。
A 瓶中装入紫色石蕊溶液,检验二氧化碳气体显酸性
B 给病人输送氧气,观察气流输出的速度
C 瓶中装入浓硫酸,用于干燥气体
D 瓶中装入氢氧化钠溶液检验二氧化碳是否存在
四、(本题共2个小题,化学方程式2分一个,其余每空1分,共16分)
13.(本题8分)项目小组对铁系食品脱氧剂(又称为“双吸剂”)进行了如下探究。
Ⅰ.探成分
某脱氧剂标签显示含有铁粉、活性炭、食盐以及无水氯化钙等。为确定脱氧剂中铁粉的存在,进行如下实验。
实验1:取一包脱氧剂粉末,用磁铁吸引。观察到部分黑色粉末被吸引。
实验2:取实验1中被吸引的部分粉末放入试管中,加入适量硫酸铜溶液。观察到有红色固体生成。
实验3:另取被磁铁吸引的黑色粉末,撒向酒精灯的火焰。观察到粉末剧烈燃烧,火星四射。
(1)写出实验2中有关反应的化学方程式: 。
(2)铁粉在空气中能燃烧,而铁丝在空气中不易被点燃。原因是 。
Ⅱ.明原理
利用图1所示装置进行实验4和实验5。
(3)实验4:一段时间后,观察到气球变大。气球变大的原因是 。
(4)实验5:能证明脱氧剂“脱氧”的现象是 。
Ⅲ.悟应用
实验6:设计如表所示对比实验探究脱氧剂中活性炭和食盐的作用。利用温度传感器测得集气瓶中温度随时间的变化曲线如图2所示。
实验序号 铁粉/g 水/mL 活性炭/g NaCl/g
① 2 5 0 0
② 2 5 0
③ 2 5 0
④ 2 5
(5)对比实验①与实验③可得到的结论是 ;对比实验③与实验④可得到的结论是 。
(6)下列叙述正确的是 (填字母)。
a.铁系食品脱氧剂可吸收氧气和水
b.铁系食品脱氧剂使用过程中放出热量
c.铁系食品脱氧剂能延长食物的保存时间
14.(本题8分)某兴趣小组对与的反应进行了探究。回答下列问题:
(1)小组同学向盛有溶液的试管中加入溶液,观察到的实验现象为 ,反应的化学方程式为 。
为确定(1)中反应后溶液的成分,小组同学开展了如下实验探究。
【提出问题】溶液中含有的溶质有哪些
【作出猜想】
(2)根据反应规律和元素守恒,提出以下猜想。
猜想一:只有;
猜想二:有和;
猜想三:有和 。
【实验探究】
(3)小组成员分别取(1)中反应后的溶液少许,置于A、B两支试管中,进行了如下实验。
实验序号 实验操作 实验现象 实验结论
Ⅰ 向试管A中加入 溶液 无明显现象 猜想二不成立
Ⅱ 向试管B中加入少量酚酞试液 无色溶液变红色
【交流讨论】
(4)有同学认为使用稀硫酸代替酚酞试液进行实验,也能得出与实验Ⅱ相同的结论。你是否同意这一观点: ;请阐述理由: 。
参考答案
题号 1 2 3 4 5 6 7 8
答案 C C A B A B C B
9.(1)b
(2)CaO+H2O=Ca(OH)2
(3)碳酸钾(碳酸氢钾或K2CO3或KHCO3)
10.(1) 肥皂水 煮沸
(2) 活性炭 +6
(3)A
(4) 氢氧化钙 蒸发结晶
(5)>
11.(1)酒精灯
(2) C b
(3)
石灰水显碱性,能使无色酚酞试液变红,溶液不变色,说明石灰水已经完全变质 BHEC
12. ⑥ 2H2O2 2H2O+ O2↑ a BC
13.(1)
(2)铁粉与氧气的接触面积大(合理即可)
(3)集气瓶内氧气被脱氧剂吸收,使瓶内气压变小
(4)打开弹簧夹后,烧杯中的水倒吸
(5) 活性炭对脱氧剂脱氧有促进作用 活性炭和氯化钠共同作用更有利于脱氧剂脱氧
(6)abc
14.(1) 产生白色沉淀
(2)/氢氧化钡
(3) (合理即可) 猜想三成立
(4) 不同意 和均可与稀硫酸反应,生成白色沉淀
展开更多......
收起↑
 资源预览
资源预览

 资源预览
资源预览


